O hipotireoidismo - diminuição da secreção de hormônio pela tireoide - pode ter diversas causas. Vamos conhecê-las:
Tireoidite autoimune crônica
Também conhecida como tireoidite de Hashimoto, é a principal causa de hipotireoidismo. Nesta doença o nosso sistema imunológico ataca indevidamente a tireoide causando sua destruição e, consequentemente, diminuição progressiva na produção hormonal.
Iatrogênico
Algumas vezes o tratamento de outras doenças acaba afetando a produção hormonal da tireoide. Por exemplo, um paciente que recebe indicação de cirurgia tireoidiana por nódulos que causam sintomas compressivos pode necessitar de reposição hormonal após o procedimento.
Também podem desenvolver hipotireoidismo pacientes que fazem tratamento de HIPERtireoidismo com iodo radioativo, ou que precisam fazer radioterapia na região da cabeça e pescoço.
Deficiência ou excesso de iodo
Nossa tireoide usa iodo para produzir o T4 e o T3 (hormônios tireoidianos). Deficiência - pouco comum no Brasil - ou excesso de iodo podem desregular a produção hormonal e induzir hipotireoidismo.
O uso de gotas de lugol ou solução SSKI por serem extremamente concentradas em iodo muitas vezes acabam desencadeando quadros de hipotireodismo em pessoas predispostas através da inibição do organificação do iodo (efeito Wolff-Chaikoff).
Medicamentos
Alguns medicamentos podem desencadear hipotireoidismo por diversos mecanismos. Destacam-se: tionamidas (propiltiuracil e metimazol), lítio, amiodarona, interferon alfa, interleucina 2, inibidores da tirosina quinase e alguns imunoterápicos (estes dois últimos são usados no tratamento de alguns tipos de câncer).
Doenças infiltrativas
Hemocromatose, tireoidite fibrosante e sarcoidose, felizmente, são causas raras de hipotireoidismo.
Hipotireoidismo transitório
Em algumas situações o quadro de hipotireoidismo é autolimitado, isto é, melhora sem tratamento após período de tempo variável.
As tireoidites silenciosa, subaguda e pós-parto são doenças que lesam o tecido tireoidiano. Como consequência, os estoques hormonais são liberados na corrente sanguínea causando HIPERtireoidismo no início do quadro. Após alguns dias ou semanas, os níveis hormonais caem e se instala o HIPOtireoidismo, que costuma ir melhorando a medida que a tireoide recupera sua capacidade de produção hormonal.
Hipotireoidismo congênito
Algumas crianças já nascem com hipotireoidismo. Má formação da tireoide ou defeitos na produção hormonal são possíveis causas. Felizmente, o teste do pezinho detecta precocemente estes casos, permitindo que o tratamento seja precoce e que se evite sequelas como retardo mental.
Hipotireoidismo central e resistência generalizada aos hormônios tireoidianos
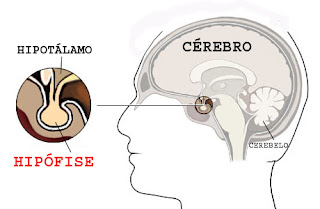
São as causas mais raras de hipotireoidismo. No hipotireoidismo central, a hipófise ou o hipotálamo não enviam a ordem (TSH ou TRH) para que a tireoide produza seus hormônios.
Já na resistência generalizada aos hormônios tireoidianos, a tireoide costuma produzir níveis elevados de hormônios. Porém os receptores hormonais localizados nos diferentes tecidos não funcionam direito. É como se a chave (T4 e T3) não encaixasse na fechadura (células do nosso organismo).
Referência:
1- Ross DS. Disorders that cause hypothyroidism. UpToDate.
Dr. Mateus Dornelles Severo
Médico Endocrinologista titulado pela SBEM
Doutor e Mestre em Endocrinologia pela UFRGS
CREMERS 30.576 - RQE 22.991
Santa Maria - RS
https://drmateusendocrino.med.br
https://drmateusendocrino.med.br